Тема: Глюкоза: молекулярна формула та її відкрита форма. Хімічні властивості глюкози.
Завдання 1. Опрацювати параграф 23.
Завдання 2. Виписати молекулярну, відкриту лінійну та циклічну формули глюкози.
Завдання 3. Виписати фізичні та хімічні властивості глюкози.
Завдання 4. Подивитись відео "Хімічні властивості глюкози".
Завдання 5. Розв'язати задачу: У якій масі води потрібно розчинити 40 г. глюкози, щоб отримати розчин із масовою часткою вуглеводу 10 %.
Завдання 6. Коротке повідомлення "Роль глюкози в організмі людини".
Виконані завдання надсилаємо особистим повідомленням в Viber протягом дня 09.02.2021. Бажаю успіхів!
Глюкоза є моносахаридом.
Молекулярна формула: С6Н12О6.
Глюкоза може існувати у двох формах:
1) відкрита
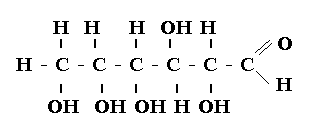
2) циклічна
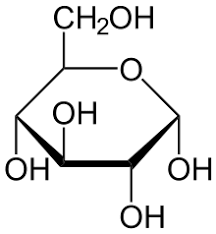
Фізичні властивості глюкози:
- безбарвна кристалічна речовина;
- без запаху;
- добре розчиняється у воді;
- погано розчиняється в органічних розчинниках;
- солодка на смак.
Хімічні властивості глюкози:
1) Реакція срібного дзеркала:
2) Якісна реакція на глюкозу - реакція із свіжоодержаним купрум (ІІ) гідроксидом. Після нагрівання розчину темно-синього кольору, утворюється червоний осад купрум (І) оксиду:
3) Відновлення - водень за наявності каталізаторів (нікель, паладій) та під дією температури відновлює альдегідну групу до гідроксильної:
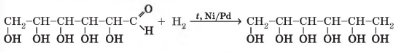
Продукт реакції - сорбіт (шестиатомний спирт) - замінник цукру.
4) Бродіння - це біохімічний процес, що відбувається під дією ферментів, які виділяють живі організми:
- спиртове бродіння: одноклітинні гриби дріжджі живляться вуглеводами, зокрема глюкозою, продуктами травлення є етанол та вуглекислий газ:
- молочнокисле бродіння: відбувається під час перероблення вуглеводів молочнокислими бактеріями, продуктом є молочна кислота:
Дата: 19.01.2021.
Тема: Естери, загальна та структурні формули, систематична номенклатура,фізичні властивості. Гідрліз естерів.
Завдання 1. Опрацювати параграф 21 та теоретичний матеріал↓.
Естери — це органічні сполуки, що утворюються внаслідок взаємодії карбонових кислоти зі спиртами з відщепленням молекули води
Загальна формула:
2. Ізомерія.
Структурна:
СН3-СН2-СО-О-СН3 – метиловий естер пропіонової кислоти
СН3-СО-О-СН2-СН3 – етиловий естер оцтової кислоти
Міжкласова:
СН3-СН2-СО-О-СН3 – метиловий естер пропіонової кислоти
СН3-СН2-СН2-СООН – масляна кислота
3. Номенклатура.
За сучасною міжнародною номенклатурою назви естерів складають з назви вуглеводневого радикала, що відповідає спирту, і кореня латинської назви кислоти з додаванням суфікса -ат.
H - CO - O - C2H5 - етилформіат (етиловий естер мурашиної кислоти);
C3H7 - CO - O - CH3 -метилбутират (метиловий естер бутанової кислоти);
C2H5 - CO - O - C3H7 - пропілпропіонат (пропіловий естер пропанової кислоти)
4. Фізичні властивості:
Гідроліз естерів — процес, протилежний реакції етерифікації.
CH3COOH ↔ CH3COO- + H+
Запам’ятайте, що під час дисоціації карбонових кислот першим завжди потрібно записувати аніон кислотного залишку, а потім катіон Гідрогену !!!
2. Дія оцтової кислоти на індикатори:
Оцтова кислота діє на індикатори як і неорганічні кислоти:
- фенолфталеїн - безбарвний;
- лакмус - червоний;
- універсальний - червоний;
- метилоранжевий - червоний
3.Взаємодія оцтової кислоти з металами:
Всі метали, що стоять у ряді активності металів до водню можуть витісняти його з оцтової кислоти.
4.Взаємодія оцтової кислоти з лугами:
Відбувається реакція нейтралізації, в результаті якої утворюється сіль та вода.
5.Взаємодія оцтової кислоти з основними та амфотерними оксидами:
6.Взаємодія оцтової кислоти зі солями:
7. Реакція відновлення:
Взаємодія з воднем при нагріванні в присутності каталізаторів, утворюються спирти:
8. Реакції естерифікації:
Якщо до оцтової кислоти додати етиловий спирт й трохи сульфатної кислоти, то при нагріванні з’являється приємний запах оцтово–етилового естеру.
9. Дія хлору на оцтову кислоту:
2. Окиснення альдегідів за схемою:
3.Мурашину кислоту добувають окисненням метану в присутності каталізатора:
4.Оцтову кислоту добувають окисненням бутану:
Тестові завдання:
1. Функціональна група карбонових кислот:
А карбонільна
Б гідроксильна
В метиленова
Г карбоксильна
5. Назва солей оцтової кислоти:
А хлориди
Б ацетати
В карбонати
Г сульфати
6. Які продукти утворюються в реакції: RCOOH + R'OH ⇔ RCOOR '+ Н2О ?
А кислота і вода
Б естер і вода
В спирт і вода
Г кислота і спирт
7. Загальна формула насичених одноосновних карбонових кислот:
А СnH2n-1СОOH
Б CnH2n+1CHO
В CnH2n+1COOH
8. Типи ізомерії насичених карбонових кислот:
А карбонового ланцюга
Б геометрична
Глюкоза може існувати у двох формах:
1) відкрита
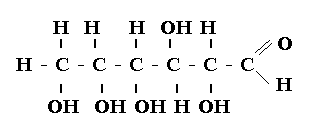
2) циклічна

Фізичні властивості глюкози:
- безбарвна кристалічна речовина;
- без запаху;
- добре розчиняється у воді;
- погано розчиняється в органічних розчинниках;
- солодка на смак.
Хімічні властивості глюкози:
1) Реакція срібного дзеркала:
C6H12O6 + Ag2O = C6H12O7 + 2Ag
2) Якісна реакція на глюкозу - реакція із свіжоодержаним купрум (ІІ) гідроксидом. Після нагрівання розчину темно-синього кольору, утворюється червоний осад купрум (І) оксиду:
С6H12O6 + 2Cu(OH)2 = C6H12O7 + 2CuOH + H2O
2CuOH = Cu2O + H2O
3) Відновлення - водень за наявності каталізаторів (нікель, паладій) та під дією температури відновлює альдегідну групу до гідроксильної:
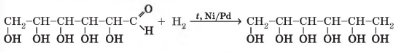
Продукт реакції - сорбіт (шестиатомний спирт) - замінник цукру.
4) Бродіння - це біохімічний процес, що відбувається під дією ферментів, які виділяють живі організми:
- спиртове бродіння: одноклітинні гриби дріжджі живляться вуглеводами, зокрема глюкозою, продуктами травлення є етанол та вуглекислий газ:
С6Н12О6 = 2С2Н5ОН + СО2
- молочнокисле бродіння: відбувається під час перероблення вуглеводів молочнокислими бактеріями, продуктом є молочна кислота:
С6Н12О6 = 2С3Н6О3
Тема: Естери, загальна та структурні формули, систематична номенклатура,фізичні властивості. Гідрліз естерів.
Завдання 1. Опрацювати параграф 21 та теоретичний матеріал↓.
Завдання 2. Виписати визначення "естери", загальну формулу естерів, номенклатуру естерів, фізичні властивості та гідроліз естерів.
Завдання 3. Навчальний міні-проект "Естери в косметиці". Звіт в довільній формі (презентація, буклет, реферат тощо).
Завдання 4. Виконати вправи 155, 156, 157 та 158 (а, б) на стор.127-128.
Виконані завдання надсилаємо особистим повідомленням в Viber до 21.01.2021. Бажаю успіхів!
Теоретичний матеріал:
Естери — це органічні сполуки, що утворюються внаслідок взаємодії карбонових кислоти зі спиртами з відщепленням молекули води
Загальна формула:
2. Ізомерія.
Структурна:
СН3-СН2-СО-О-СН3 – метиловий естер пропіонової кислоти
СН3-СО-О-СН2-СН3 – етиловий естер оцтової кислоти
Міжкласова:
СН3-СН2-СО-О-СН3 – метиловий естер пропіонової кислоти
СН3-СН2-СН2-СООН – масляна кислота
3. Номенклатура.
За сучасною міжнародною номенклатурою назви естерів складають з назви вуглеводневого радикала, що відповідає спирту, і кореня латинської назви кислоти з додаванням суфікса -ат.
замісник + алкан + оат (метил + пропан + оат)
Наприклад:H - CO - O - C2H5 - етилформіат (етиловий естер мурашиної кислоти);
C3H7 - CO - O - CH3 -метилбутират (метиловий естер бутанової кислоти);
C2H5 - CO - O - C3H7 - пропілпропіонат (пропіловий естер пропанової кислоти)
4. Фізичні властивості:
- Естери нижчих карбонових кислот і спиртів – безбарвні леткі рідини з приємним фруктовим запахом.
- Естери мінеральних кислот – маслянисті рідини з приємним запахом.
- Естери вищих спиртів і вищих карбонових кислот – тверді речовини, що майже не мають запаху. Вони мало розчинні у воді і добре – в спирті та інших органічних розчинниках.
5. Гідроліз естерів.
Гідроліз естерів (омилення) - реакція взаємодії естерів з водою за наявності неорганічної кислоти (або лугу), за якої утворюються кислота та спирт.
Дата: 15.01.2021.
Тема: Хімічні властивості насичених одноосновних карбонових кислот. Реакція естерифікації. Одержання етанової кислоти.
Завдання 1. Виписати хімічні властивості насичених одноосновних карбонових кислот↓.
Завдання 2. Переглянути відео "Хімічні властивості карбонових кислот".
Завдання 3. Виконати тестові завдання 1-12↓.
Виконані завдання надсилаємо особистим повідомленням в Viber до 18.01.2021. Бажаю успіхів!
Відео "Хімічні властивості карбонових кислот"
Хімічні властивості насичених одноосновних карбонових кислот на прикладі оцтової кислоти:
1.Електролітична дисоціація:CH3COOH ↔ CH3COO- + H+
Запам’ятайте, що під час дисоціації карбонових кислот першим завжди потрібно записувати аніон кислотного залишку, а потім катіон Гідрогену !!!
2. Дія оцтової кислоти на індикатори:
Оцтова кислота діє на індикатори як і неорганічні кислоти:
- фенолфталеїн - безбарвний;
- лакмус - червоний;
- універсальний - червоний;
- метилоранжевий - червоний
3.Взаємодія оцтової кислоти з металами:
Всі метали, що стоять у ряді активності металів до водню можуть витісняти його з оцтової кислоти.
CH3COOH + Zn = (CH3COO)2 Zn + Н2↑
Відбувається реакція нейтралізації, в результаті якої утворюється сіль та вода.
CH3COOH + КОН → CH3COOК + H2О
5.Взаємодія оцтової кислоти з основними та амфотерними оксидами:
2CH3COOH + СаО → (CH3COO)2Са + H2О
6.Взаємодія оцтової кислоти зі солями:
2CH3COOH + Nа2CО3 →2CH3COONа + CO2↑ + H2О
7. Реакція відновлення:
Взаємодія з воднем при нагріванні в присутності каталізаторів, утворюються спирти:
СН3COOH + 2Н2 → CH3CН2OН (етанол) + Н2О
8. Реакції естерифікації:
Якщо до оцтової кислоти додати етиловий спирт й трохи сульфатної кислоти, то при нагріванні з’являється приємний запах оцтово–етилового естеру.
СН3COOH + НO–С2Н5 → CH3COOC2Н5 (оцтово-етиловий естер) + H2O.
9. Дія хлору на оцтову кислоту:
CH3COOH + Cl2 → CH2ClCOOН + HCl
Добування карбонових кислот:
1. Окиснення спиртів:
1. Окиснення спиртів:
R-ОН + О2→RСООН +Н2О
2. Окиснення альдегідів за схемою:
2R-СНО + О2→2R-СООН
3.Мурашину кислоту добувають окисненням метану в присутності каталізатора:
2СН4 + О2→2НСООН +Н2О
4.Оцтову кислоту добувають окисненням бутану:
2С4Н10 +5О2 → 4 CH3COOH + Н2О
Тестові завдання:
1. Функціональна група карбонових кислот:
А карбонільна
Б гідроксильна
В метиленова
Г карбоксильна
2. При взаємодії оцтової кислоти з металами виділяється газ:
А хлор
Б кисень
В водень
Г хлороводень
3. Назва реакції оцтової кислоти з лугом:
А нейтралізація
Б заміщення
В хлорування
Г обміну
4. Назва реакції карбонової кислоти із спиртом:
А обмін
Б естерифікація
В заміщення
Г етерифікація
А хлор
Б кисень
В водень
Г хлороводень
3. Назва реакції оцтової кислоти з лугом:
А нейтралізація
Б заміщення
В хлорування
Г обміну
4. Назва реакції карбонової кислоти із спиртом:
А обмін
Б естерифікація
В заміщення
Г етерифікація
5. Назва солей оцтової кислоти:
А хлориди
Б ацетати
В карбонати
Г сульфати
6. Які продукти утворюються в реакції: RCOOH + R'OH ⇔ RCOOR '+ Н2О ?
А кислота і вода
Б естер і вода
В спирт і вода
Г кислота і спирт
7. Загальна формула насичених одноосновних карбонових кислот:
А СnH2n-1СОOH
Б CnH2n+1CHO
В CnH2n+1COOH
8. Типи ізомерії насичених карбонових кислот:
А карбонового ланцюга
Б геометрична
В міжкласова
Г положення кратного звязку
9. Мило - це:
А солі карбонових кислот і лужних металів.
Б солі вищих карбонових кислот і лужних металів
В солі гліцеролу і лужних металів.
Г солі вищих карбонових кислот і металів.
Г положення кратного звязку
9. Мило - це:
А солі карбонових кислот і лужних металів.
Б солі вищих карбонових кислот і лужних металів
В солі гліцеролу і лужних металів.
Г солі вищих карбонових кислот і металів.
10. Якого кольору набуває лакмус в розчині етанової кислоти?
А червоного
Б синього
В жовтого
Г оранжевого
А червоного
Б синього
В жовтого
Г оранжевого
11. Яка з цих кислот є сильним електролітом?
А мурашина
Б оцтова
В масляна
Г валеріанова
А мурашина
Б оцтова
В масляна
Г валеріанова
12. Реакція естерифікації - це взаємодія карбонових кислот з:
А металами
Б основами
А металами
Б основами
В спиртами
Г солями
Дата: 12.01.2021.
Тема: Карбонові кислоти, їх поширення в природі та класифікація. Карбоксильна характеристична (функціональна) група. Склад, будова молекул насичених одноосновних карбонових кислот, їхня загальна та структурні формули, ізомерія, систематична номенклатура і фізичні властивості.
Завдання 1: Опрацювати параграф 18 та теоретичний матеріал ↓. Виписати в зошит визначення карбонових кислот, загальну формулу карбонових кислот, функціональну групу та гомологічний ряд (з таблички).
Завдання 2: Виконати вправи № 130, 131 на стор.113-114.
Тема: Карбонові кислоти, їх поширення в природі та класифікація. Карбоксильна характеристична (функціональна) група. Склад, будова молекул насичених одноосновних карбонових кислот, їхня загальна та структурні формули, ізомерія, систематична номенклатура і фізичні властивості.
Завдання 1: Опрацювати параграф 18 та теоретичний матеріал ↓. Виписати в зошит визначення карбонових кислот, загальну формулу карбонових кислот, функціональну групу та гомологічний ряд (з таблички).
Завдання 2: Виконати вправи № 130, 131 на стор.113-114.
Виконані завдання надсилаємо особистим повідомленням в Viber до 14.01.2021. Бажаю успіхів!
Теоретичний матеріал:
1. Поширення в природі:
4. Класифікація карбонових кислот:
а) залежно від кількості карбоксильних груп у молекулі — на одноосновні, двохосновні та багатоосновні:
б) залежно від природи радикала — на насичені, ненасичені й ароматичні
5. Гомологічний ряд й номенклатура карбонових кислот.
Назва кислоти походить від назви відповідного вуглеводню: до назви алкана додають суфікс -ов- і закінчення -а та слово кислота (етанова кислота). У зв'язку з тим що багато карбонових кислот було відкрито задовго до прийняття правил міжнародної номенклатури, більшість з них мають традиційні (тривіальні) назви.
Теоретичний матеріал:
1. Поширення в природі:
Мурашина кислота виробляється мурахами, міститься в кропиві і хвої ялини.
Масляна кислота – утворюється у разі прогіркання масла, є запахом поту.
Ізовалеріанова кислота – в коренях валеріани лікарської.
Стеаринова і пальмітинова кислота – пальмова олія.
Стеаринова і пальмітинова кислота – пальмова олія.
Щавлева кислота - в щавлі, ревені, кислиці, шпинаті.
Яблучна кислота – яблука.
Лимонна кислота - апельсин, грейпфрут, лимон.
Оцтова кислота – утворюється при прокисанні вина
2. Поняття про карбонові кислоти.
2. Поняття про карбонові кислоти.
Карбонові кислоти — це органічні речовини, молекули яких містять одну або кілька карбоксильних груп, сполучених з вуглеводневим радикалом.
3. Функціональна група й будова карбонових кислот.
Загальна формула карбонових кислот:
3. Функціональна група й будова карбонових кислот.
Загальна формула карбонових кислот:
СnH2n+1COOH або R – COOH
4. Класифікація карбонових кислот:
а) залежно від кількості карбоксильних груп у молекулі — на одноосновні, двохосновні та багатоосновні:
б) залежно від природи радикала — на насичені, ненасичені й ароматичні
5. Гомологічний ряд й номенклатура карбонових кислот.
Назва кислоти походить від назви відповідного вуглеводню: до назви алкана додають суфікс -ов- і закінчення -а та слово кислота (етанова кислота). У зв'язку з тим що багато карбонових кислот було відкрито задовго до прийняття правил міжнародної номенклатури, більшість з них мають традиційні (тривіальні) назви.
6. Фізичні властивості карбонових кислот.
Нижчі карбонові кислоти — рідини з гострим запахом, добре розчинні у воді. З підвищенням відносної молекулярної маси розчинність кислот у воді зменшується, а температура кипіння підвищується. Вищі кислоти, починаючи з нонановоїСН3—(СН2)7—СООН,— тверді речовини, без запаху, нерозчинні у воді.
Дата: 29.12.2020.
Тема: Контрольна робота з хімії за І семестр.
Виконану контрольну роботу надсилаємо особистим повідомленням в Viber до 30.12.2020.
1. Вкажіть загальну формулу алкенів:
7. Складіть структурні формули за назвами алканів:
а) 3-етил- 1,2 – диметил пент-1-ен;
Виконану контрольну роботу надсилаємо особистим повідомленням в Viber до 30.12.2020.
Контрольна робота з хімії за І семестр
І рівень
(1 бал за кожну правильну відповідь)
а) СnН2n-2; б) СnН2n+2;
в) СnН2n; г) СnН2n-6.
2. Укажіть формулу найближчого гомолога етену:
а) С7Н14; б) СзН6;
в) СзН4; г) СН4.
3. Під час гідрування етену утворюється:
а) етин; б) етанол;
в) етан; г) етаналь.
4. Укажіть, до якого типу належить реакція брому з етеном:
а) приєднання; б) розкладу;
в) обміну; г) заміщення.
5. Реакція приєднання води називається:
а) дегідратація; б) гідрування;
в) гідратація; г) дегідрування.
6. Укажіть формулу алкану, який містить 13 атомів Карбону:
в) СnН2n; г) СnН2n-6.
2. Укажіть формулу найближчого гомолога етену:
а) С7Н14; б) СзН6;
в) СзН4; г) СН4.
3. Під час гідрування етену утворюється:
а) етин; б) етанол;
в) етан; г) етаналь.
4. Укажіть, до якого типу належить реакція брому з етеном:
а) приєднання; б) розкладу;
в) обміну; г) заміщення.
5. Реакція приєднання води називається:
а) дегідратація; б) гідрування;
в) гідратація; г) дегідрування.
6. Укажіть формулу алкану, який містить 13 атомів Карбону:
а) С13Н28; б) С13Н26;
в) С12Н24; г) С12Н20.
в) С12Н24; г) С12Н20.
ІІ рівень
(3 бали)
а) 3-етил- 1,2 – диметил пент-1-ен;
б) 4-етил,5-метилгептан.
8. Написати рівняння реакцій для наступних перетворень (не забуваємо ставити коефіцієнти):
а) СН4 → СН3Br
б) С5Н12→ СО2 + Н2О
в) С2Н4 → С2Н5ОН
ІІІ рівень
(3 бали)
9. До складу молекули алкену входить 8 атомів Карбону. Користуючись загальною формулою гомологічного ряду, встановіть склад молекули алкену, виведіть його молекулярну формулу та дайте назву, обчисліть масові частки хімічних елементів, що входять до складу молекули даного алкену.
Дата: 22.12.2020.
а) гліцерил; б) бутанол; в) пентанол.
3. Що є спільне у будові насичених одноатомних, багатоатомних спиртів, фенолу:
а) наявність вуглеводневих радикалів насиченого складу;
б) наявність ароматичного радикала;
в) наявність характеристичних гідроксильних груп.
4. Внаслідок взаємодії насичених альдегідів із воднем утворюються:
Тема: Узагальнення та систематизація знань з теми «Оксигеновмісні органічні сполуки: спирти, фенол, альдегіди».
Виконані завдання 1-7 (тести) та 8-30 (дати відповіді на питання) надсилаємо особистим повідомленням в Viber до 28.12.2020.
1. Яка з формул виражає загальну формулу насичених одноатомних спиртів:
а) CnH2n+2 б) CnH2n+1-COH в) CnH2n+1-OH
2. Виберіть формулу спирту, що застосовують у парфумерії для виробництва кремів:
1. Яка з формул виражає загальну формулу насичених одноатомних спиртів:
а) CnH2n+2 б) CnH2n+1-COH в) CnH2n+1-OH
2. Виберіть формулу спирту, що застосовують у парфумерії для виробництва кремів:
а) гліцерил; б) бутанол; в) пентанол.
3. Що є спільне у будові насичених одноатомних, багатоатомних спиртів, фенолу:
а) наявність вуглеводневих радикалів насиченого складу;
б) наявність ароматичного радикала;
в) наявність характеристичних гідроксильних груп.
4. Внаслідок взаємодії насичених альдегідів із воднем утворюються:
а) етери; б) насичені одноатомні спирти; в) карбонові кислоти.
5. Яка з властивостей фенолу спричинила застосування його розчину у медицині:
а) легко розчиняється у воді;
б) має різкий неприємний запах;
в) вбиває бактерії, є сильний антисептик.
6. Яка речовина має практичне застосування в медицині та піротехніці:
5. Яка з властивостей фенолу спричинила застосування його розчину у медицині:
а) легко розчиняється у воді;
б) має різкий неприємний запах;
в) вбиває бактерії, є сильний антисептик.
6. Яка речовина має практичне застосування в медицині та піротехніці:
а) гліцерил; б) етанол; в) нітрогліцерол.
7. Як називається функціональна група спиртів:
а) карбонільна; б) гідроксильна; в) карбоксильна.
8. Як називається розділ загальної хімії,що вивчає органічні речовини?
9. Назвіть видатного українського хіміка, який сформулював основні положення теорії будови органічних речовин.
10. За якою ознакою ароматичні вуглеводні отримали назву ароматичні?
11. Який хімічний елемент, крім С і Н входить до складу спиртів?
12. Який спирт дуже широко використовують у парфумерії і медицині?
13. Яка загальна формула насичених одноатомних спиртів?
14. Який суфікс бере участь в утворенні назви одноатомних насичених спиртів?
15. Яка буде назва одноатомного насиченого спирту,якщо його вуглецевий ланцюг складається з восьми атомів?
16. З якою кислотою взаємодіятиме гліцерол, щоб утворився 1,2,3-тринітрогліцерол? 17. Який газ утворюється під чаc повного горіння будь-якого спирту?
18. Що називають реакцією дегідратації?
19. Який спирт утворюється при гідратації бут -2-ену?
20. Який спирт отримують в результаті бродіння харчової сировини та рослинних матеріалів?
21. Яка речовина крім спирту утворюється в результаті бродіння?
22. При взаємодії з якими металами утворюються алкоголяти?
23. Які види ізомерії характерні для одноатомних насичених спиртів?
24. Назвіть трьохатомний спирт.
27. Ще таке антифризи?
28. З яких двох частин складається молекула фенолу?
29. Як називаються речовини,які мають однаковий якісний і кількісний склад,а різну будову молекули?
30. Вживання невеликої кількості якого спирту викликає сліпоту, а понад 25мл – смерть?
7. Як називається функціональна група спиртів:
а) карбонільна; б) гідроксильна; в) карбоксильна.
8. Як називається розділ загальної хімії,що вивчає органічні речовини?
9. Назвіть видатного українського хіміка, який сформулював основні положення теорії будови органічних речовин.
10. За якою ознакою ароматичні вуглеводні отримали назву ароматичні?
11. Який хімічний елемент, крім С і Н входить до складу спиртів?
12. Який спирт дуже широко використовують у парфумерії і медицині?
13. Яка загальна формула насичених одноатомних спиртів?
14. Який суфікс бере участь в утворенні назви одноатомних насичених спиртів?
15. Яка буде назва одноатомного насиченого спирту,якщо його вуглецевий ланцюг складається з восьми атомів?
16. З якою кислотою взаємодіятиме гліцерол, щоб утворився 1,2,3-тринітрогліцерол? 17. Який газ утворюється під чаc повного горіння будь-якого спирту?
18. Що називають реакцією дегідратації?
19. Який спирт утворюється при гідратації бут -2-ену?
20. Який спирт отримують в результаті бродіння харчової сировини та рослинних матеріалів?
21. Яка речовина крім спирту утворюється в результаті бродіння?
22. При взаємодії з якими металами утворюються алкоголяти?
23. Які види ізомерії характерні для одноатомних насичених спиртів?
24. Назвіть трьохатомний спирт.
27. Ще таке антифризи?
28. З яких двох частин складається молекула фенолу?
29. Як називаються речовини,які мають однаковий якісний і кількісний склад,а різну будову молекули?
30. Вживання невеликої кількості якого спирту викликає сліпоту, а понад 25мл – смерть?
Дата: 28.05.2020.
Тема: Урок узагальнення та систематизації вивченого матеріалу за рік.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 29.05.2020.
Завдання: розв'язати кросворд.
Дата: 25.05.2020.
Тема: Урок узагальнення та систематизації знань за ІІ семестр.
Завдання: дайте короткі відповіді на питання 1-20.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 27.05.2020.
Дата: 21.05.2020.
Тема: Зв’язки між класами органічних речовин. Роль органічної хімії у розв’язуванні сировинної, енергетичної та продовольчої проблем і створенні нових матеріалів.
Завдання: виконати вправи 1, 2, 3.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 22.05.2020.
1. Класифікуйте органічні речовини на класи (алкани, алкени, алкіни, спирти, карбонові кислоти) за їхніми молекулярними формулами. Назвіть ці речовини.
С4Н8,
С2Н5СООН,
С5Н11ОН,
С2Н2,
С3Н7ОН,
С6Н14,
С3Н5(ОН)3,
СН3СООН;
С4Н9СООН.
2. Складіть структурні формули органічних речовин за їхніми назвами:
а) 2,2- диметилпропан;
б) 3-етилпент-2-ен;
в) 1,1,2-трибромопропан;
г) 3-метилбут-1-ин;
д) пентан-2-ол;
ж) пентанова кислота.
3. Назвіть речовини за їхніми структурними формулами:
Дата: 18.05.2020.
Тема: Загальні поняття про біологічно активні речовини (вітаміни, ферменти).
Завдання 1. Опрацювати §36.
Завдання 2. Виписати терміни "біологічно активні речовини", "вітаміни", "ферменти".
Завдання 3. Виконати вправи 262, 263, 264, 265 (стор. 218).
Виконанні завдання надсилаємо особистим повідомленням в Viber до 20.05.2020.
Біологічно активні речовини — це органічні сполуки різної хімічної природи, здатні впливати на обмін речовин та перетворення енергії в живих істотах. До біологічно активних речовин належать ферменти, вітаміни, гормони, нейрогормони, фактори росту, фіто- гормони, антибіотики тощо.
Вітаміни — органічні речовини, що надходять в організм людини з їжею і забезпечують нормальний обмін речовин, його фізіологічне функціонування.
Ферменти — група речовин переважно білкової природи, які виконують роль каталізаторів біохімічних реакцій в організмах.
Дата: 14.05.2020.
Тема: Контрольна робота № 2.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 14.05.2020.
Дата: 07.05.2020.
Тема: Синтетичні волокна: фізичні властивості і застосування.
Завдання 2. Виписати термін "синтетичні волокна" і оформити схему "Класифікація волокон".
Завдання 3. Тестові завдання 1-6.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 08.05.2020.
Синтетичні волокна — це хімічні волокна, що формуються із синтетичних полімерів.
Дата: 04.05.2020.
Тема: Найпоширеніші полімери та сфери їхнього використання. Вплив полімерних матеріалів на здоров’я людини і довкілля. Проблеми утилізації полімерів і пластмас в контексті сталого розвитку суспільства.
Мета: формувати знання учнів про синтетичні високомолекулярні речовини, полімери, реакції полімеризації і поліконденсації, пластмаси, каучуки і гуму та сфери їх використання.
Завдання 1. Опрацювати § 30.
Завдання 2. Підготувати навчальний проект на одну з тем:
Виконанні завдання надсилаємо особистим повідомленням в Viber до 08.05.2020.
Дата: 30.04.2020.
Тема: Синтетичні високомолекулярні речовини. Полімери. Реакції полімеризації і поліконденсації. Пластмаси. Каучуки, гума.
Мета: формувати знання учнів про синтетичні високомолекулярні речовини, полімери, реакції полімеризації і поліконденсації, пластмаси, каучуки і гуму та сфери їх використання.
Завдання 1. Виписати терміни: полімери, полімеризація, поліконденсація, каучук, гума.
Завдання 2. Розвяжіть задачу, використовуючи загальну формулу полімерів.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 04.05.2020.
Полімери — природні та штучні сполуки, молекули яких складаються з великого числа повторюваних однакових або різних за будовою атомних угруповань, сполучених між собою в довгі лінійні або розгалужені ланцюги.
Дата: 16.04.2020.
Тема: Амінокислоти: склад і будова молекул, загальні і структурні формули, характеристичні (функціо-нальні) групи, систематична номенклатура. Пептидна група. Хімічні властивості аміноетанової кислоти. Пептиди.
Мета: вивчити склад, будову, властивості амінокислот.
Завдання 1. Опрацювати теоретичний матеріал і оформити конспект уроку.
Завдання 2. Виконати вправи.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 21.04.2020.
Теоретичний матеріал:
Амінокислоти – це амфотерні органічні сполуки, в молекулах яких міститься одночасно аміногрупа -NH2 й карбоксильна група – COOH.
Загальна формула амінокислот:
Мета: поглибити поняття про білки як природні полімери; вивчити склад, будову білкових молекул; ознайомити учнів з властивостями білків.
Завдання 1. Опрацювати теоретичний матеріал і оформити конспект уроку.
Завдання 2. Виконати завдання самостйної роботи.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 26.04.2020.
Теоретичний матеріал:
Тема: Урок узагальнення та систематизації вивченого матеріалу за рік.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 29.05.2020.
Завдання: розв'язати кросворд.
1.
Структурна одиниця
молекули білка.
2.
Третинна структура
білка.
3.
Просторова фігура,
що відображає вторинну структуру білка.
4.
Зв'язок за допомогою
якого амінокислоти сполучаються в молекулу білка.
5.
Процес руйнування
вторинної і третинної структури білка.
6.
Каталізатори, що пришвидшують
хімічні реакції в живому організмі.
7.
Білок крові який
переносить до тканин кисень.
8.
Загальна назва
білків, які можуть руйнувати та зв’язувати бактерії, віруси тощо.
9.
Хімічний елемент,
який складає основу білків.
10. Біополімер, який складається зі з’єднаних у
певній послідовності залишків амінокислот.
11. Зв'язок між окремими поліпептидними ланцюгами.
12. Якісна реакція на білок за допомогою солей
Купруму в лужному середовищі.
Дата: 25.05.2020.
Тема: Урок узагальнення та систематизації знань за ІІ семестр.
Завдання: дайте короткі відповіді на питання 1-20.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 27.05.2020.
1. Як називається розділ загальної хімії,що вивчає органічні речовини?
2. За якою ознакою ароматичні вуглеводні отримали назву ароматичні?
3. Який хімічний елемент, крім С і Н входить до складу спиртів?
5. Який спирт дуже широко використовують у парфумерії і медицині?
6. Яка загальна формула насичених одноатомних спиртів?
7. Який суфікс бере участь в утворенні назви одноатомних насичених спиртів?
8. Яка буде назва одноатомного насиченого спирту,якщо його вуглецевий ланцюг складається з восьми атомів?
9. З якою кислотою взаємодіятиме гліцерол, щоб утворився 1,2,3-тринітрогліцерол?
10. Який газ утворюється під чаc повного горіння будь-якого спирту?
11. Що називають реакцією дегідратації?
12. Які речовини утворюється в результаті бродіння?
13. Як називають двоатомні спирти?
14. Який суфікс використовується при номенклатурі трьохатомних спиртів?
15. Ще таке антифризи?
16. З яких двох частин складається молекула фенолу?
16. З яких двох частин складається молекула фенолу?
17. Як називаються речовини,які мають однаковий якісний і кількісний склад,а різну будову молекули?
18. Що таке реакція бромування?
18. Що таке реакція бромування?
19. Вживання невеликої кількості якого спирту викликає сліпоту, а понад 25мл – смерть?
20. Яка тривіальна (історична) назва етилового спирту ?
Дата: 21.05.2020.
Тема: Зв’язки між класами органічних речовин. Роль органічної хімії у розв’язуванні сировинної, енергетичної та продовольчої проблем і створенні нових матеріалів.
Завдання: виконати вправи 1, 2, 3.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 22.05.2020.
1. Класифікуйте органічні речовини на класи (алкани, алкени, алкіни, спирти, карбонові кислоти) за їхніми молекулярними формулами. Назвіть ці речовини.
С4Н8,
С2Н5СООН,
С5Н11ОН,
С2Н2,
С3Н7ОН,
С6Н14,
С3Н5(ОН)3,
СН3СООН;
С4Н9СООН.
2. Складіть структурні формули органічних речовин за їхніми назвами:
а) 2,2- диметилпропан;
б) 3-етилпент-2-ен;
в) 1,1,2-трибромопропан;
г) 3-метилбут-1-ин;
д) пентан-2-ол;
ж) пентанова кислота.
3. Назвіть речовини за їхніми структурними формулами:
Дата: 18.05.2020.
Тема: Загальні поняття про біологічно активні речовини (вітаміни, ферменти).
Завдання 1. Опрацювати §36.
Завдання 2. Виписати терміни "біологічно активні речовини", "вітаміни", "ферменти".
Завдання 3. Виконати вправи 262, 263, 264, 265 (стор. 218).
Виконанні завдання надсилаємо особистим повідомленням в Viber до 20.05.2020.
Біологічно активні речовини — це органічні сполуки різної хімічної природи, здатні впливати на обмін речовин та перетворення енергії в живих істотах. До біологічно активних речовин належать ферменти, вітаміни, гормони, нейрогормони, фактори росту, фіто- гормони, антибіотики тощо.
Вітаміни — органічні речовини, що надходять в організм людини з їжею і забезпечують нормальний обмін речовин, його фізіологічне функціонування.
Ферменти — група речовин переважно білкової природи, які виконують роль каталізаторів біохімічних реакцій в організмах.
Дата: 14.05.2020.
Тема: Контрольна робота № 2.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 14.05.2020.
Контрольна робота з хімії № 2.
І рівень
(6 балів)
1. Жир – це
… :
а)
естер, утворений етиловим спиртом і мурашиною кислотою;
б)
естер, утворений вищими карбоновими кислотами і гліцерином;
в)
естер двохатомного спирту і карбонової кислоти;
г)
естер, утворений гліцерином і етановою кислотою.
2. Укажіть формулу гліцеролу:
а)
СН3—О—СН3;
б)
СН3СООН;
в)
СН2ОН—СНОН—СН2ОН;
г)
С2Н5ОН.
3. Під час гідрування жирів
відбувається хімічна реакція, яка використовується для:
а) перетворення рідких
жирів у тверді жири;
б) перетворення твердих
жирів у рідкі жири;
в) виготовлення вершкового
масла.
г) виготовлення маргарину.
4.
Визначте, до якого класу органічних сполук належать
мила:
а) спирти;
б) естери;
в) карбонові
кислоти.
5. У складі спиртів є така функціональна група:
а) -CH2;
б) -OH;
в) -СООН;
г) -СНО.
6. До складу карбонових кислот входить група:
а) карбонільна;
б) карбоксильна;
в) гідроксильна.
ІІ рівень (3 бали)
7. Установіть відповідність між назвою вуглеводу та назвою групи
вуглеводів, до якої його відносять:
Вуглевод Група
вуглеводів
А
Фруктоза
1 Полісахариди
Б
Крохмаль
2 Дисахариди
В
Сахароза 3 Моносахариди
9.Обчислити відносну молекулярну масу глюкози.
ІІІ рівень (3 бали)
8. Запишіть структурні формули речовин за їх назвами:
1) 3-етил-2,4-диметилпентанова кислота;
2) 2,3,4-триметилдекан;
3) 2-етил-3,4-диметилгекс-4-ол.
Дата: 07.05.2020.
Тема: Синтетичні волокна: фізичні властивості і застосування.
Завдання 2. Виписати термін "синтетичні волокна" і оформити схему "Класифікація волокон".
Завдання 3. Тестові завдання 1-6.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 08.05.2020.
Синтетичні волокна — це хімічні волокна, що формуються із синтетичних полімерів.
1. Позначте назву процесу утворення полімеру з мономеру:
А гідроліз;
полімеризація;
денатурація;
деструкція.
Тема: Найпоширеніші полімери та сфери їхнього використання. Вплив полімерних матеріалів на здоров’я людини і довкілля. Проблеми утилізації полімерів і пластмас в контексті сталого розвитку суспільства.
Мета: формувати знання учнів про синтетичні високомолекулярні речовини, полімери, реакції полімеризації і поліконденсації, пластмаси, каучуки і гуму та сфери їх використання.
Завдання 1. Опрацювати § 30.
Завдання 2. Підготувати навчальний проект на одну з тем:
- Переробка побутових відходів в Україні та розвинених країнах світу.
- Дослідження маркування виробів із полімерних матеріалів і пластмас.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 08.05.2020.
Дата: 30.04.2020.
Тема: Синтетичні високомолекулярні речовини. Полімери. Реакції полімеризації і поліконденсації. Пластмаси. Каучуки, гума.
Мета: формувати знання учнів про синтетичні високомолекулярні речовини, полімери, реакції полімеризації і поліконденсації, пластмаси, каучуки і гуму та сфери їх використання.
Завдання 1. Виписати терміни: полімери, полімеризація, поліконденсація, каучук, гума.
Завдання 2. Розвяжіть задачу, використовуючи загальну формулу полімерів.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 04.05.2020.
Полімери — природні та штучні сполуки, молекули яких складаються з великого числа повторюваних однакових або різних за будовою атомних угруповань, сполучених між собою в довгі лінійні або розгалужені ланцюги.
Полімеризація — це послідовне сполучення однакових молекул низькомолекулярної речовини з утворенням високомолекулярної речовини.
Поліконденсація — це процес утворення високомолекулярних сполук з низькомолекулярних, що зазвичай супроводжується виділенням побічних речовин (води, амоніаку, хлороводню тощо).
Каучуки — це еластичні матеріали, з яких методом вулканізації (нагріванням із сіркою) дістають гуму. Каучуки бувають природними та синтетичними.
Гума — це вулканізований сіркою каучук.
Задача: Визначте ступінь полімеризації поліетилену, відносна молекулярна маса якого складає 145 600.
Дата: 16.04.2020.
Тема: Амінокислоти: склад і будова молекул, загальні і структурні формули, характеристичні (функціо-нальні) групи, систематична номенклатура. Пептидна група. Хімічні властивості аміноетанової кислоти. Пептиди.
Мета: вивчити склад, будову, властивості амінокислот.
Завдання 1. Опрацювати теоретичний матеріал і оформити конспект уроку.
Завдання 2. Виконати вправи.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 21.04.2020.
Теоретичний матеріал:
Амінокислоти – це амфотерні органічні сполуки, в молекулах яких міститься одночасно аміногрупа -NH2 й карбоксильна група – COOH.
Загальна формула амінокислот:
Фізичні властивості:
Амінокислоти – це тверді, безбарвні,
кристалічні речовини, більшість з яких добре розчинні у воді. Багато з них
солодкі на смак. Відомо близько 200 амінокислот, з них в складі білків тіла людини їх – 20.
Амінооцтова кислота – найпростіша з
амінокислот. Водний розчин цієї амінокислоти має нейтральну реакцію, оскільки у
кислоті міститься одна аміногрупа, яка проявляє лужні властивості й одна
карбоксильна група, яка проявляє кислотні властивості.
Хімічні
властивості:
1. Взаємодія з хлоридною кислотою.
2. Взаємодія з сульфатною кислотою.
3. Реакція з оксидами, гідроксидами й
солями.
4. Реакція із спиртами з утворенням
естерів.
5.
Найважливішою властивістю амінокислот є взаємодія їх молекул між собою, яка
відбувається за рахунок різних за характером функціональних груп. Унаслідок
реакцій утворюються ди–, три–, поліпептиди й виділяється вода:
Група атомів
–C–N–, яка сполучає окремі ланки ланцюга в такій молекулі,
називається пептидною, а зв’язок між атомами Карбону й Нітрогену – пептидний.
Такий зв’язок характерний лише для білків. Дипептид, що утворився може
реагувати з третьою молекулою амінокислоти з утворенням трипептиду й т. д.
Утворена молекула побудована із залишків α-амінокислот називається
поліпептидом.
Значення
амінокислот
1. Із амінокислот в організмі
синтезуються білки органів й тканин, гормони, ферменти та інші біологічно
важливі речовини. Амінокислоти використовують як лікувальні засоби при деяких
захворюваннях: метіонін – при церозі печінки, після операції на серці, при
інфаркті; лізин – харчування для недоношених дітей, для підгодівлі тварин у
сільському господарстві; глютамінова кислота – при епілепсії.
2. Для виробництва синтетичних
волокон, наприклад, капрону й енанту.
Вправи:
1. Зобразіть структурні формули
амінокислот складу: С4Н9О2N.
2. Закінчіть рівняння реакції:
NH2–CH2–CH2–COOH + HCI →
3. Доповни
речення:
Амінокислоти
– це ___________органічні сполуки, в молекулах яких міститься одночасно _______
й __________. Поліпептиди
характеризуються наявністю зв’язку -NH-СО- , який називається ___________. Амінокислоти,
які синтезуються в організмі тварин й людини, називають __________.
Амінокислоти, які не синтезуються в організмі, а надходять з їжею, називають _______.
Дата: 23.04.2020.
Тема: Білки як
високомолекулярні сполуки. Хімічні властивості білків (без запису рівнянь
реакцій).Мета: поглибити поняття про білки як природні полімери; вивчити склад, будову білкових молекул; ознайомити учнів з властивостями білків.
Завдання 1. Опрацювати теоретичний матеріал і оформити конспект уроку.
Завдання 2. Виконати завдання самостйної роботи.
Виконанні завдання надсилаємо особистим повідомленням в Viber до 26.04.2020.
Теоретичний матеріал:
Білки – це складні високомолекулярні природні
сполуки, побудовані із залишків амінокислот з’єднаних у певні послідовності пептидними зв’язками.
Білкові молекули мають чотири рівні
структурної організації:
• первинна (послідовність амінокислот, з’єднаних між собою поліпептидним
зв’язком);
• вторинна (впорядковане розташування окремих ділянок
поліпептидного ланцюга у вигляді спіралей або складок);
• третинна (скручування молекули вторинної структури у
клубок);
• четвертинна (формується кількома молекулами третинної структури,
утворюючи стійкий комплекс).
Класифікація білків:
1. За хімічним складом:
Прості (протеїни) – складаються з амінокислот.
Складні (протеїди) – крім амінокислот містять компоненти небілкової природи (вуглеводи, ортофосфорну
кислоту, нуклеїнові кислоти.)
2. За фізіологічними
функціями:
Фібрилярні – пучки ниток (ниткоподібні) з
них будуються волокна живих тканин.
Глобулярні – вигляд клубка (кулясті), підтримують
і регулюють життєві процеси.
Самостійна робота:
1.
У
складі волосся, рогів, копит, є білок:
а)
гемоглобін в) міоглобін
б)
альбумін г) кератин
2.
Незамінні
амінокислоти – це:
А 20 різних амінокислот, які входять до складу природних
білків
Б такі, що не синтезуються в організмі тварини
В такі, що не синтезуються в організмі рослини
Г 10 різних амінокислот, які мають основні властивості
3.
Мономерами білка є:
А
амінокислоти;
Б
моносахариди;
В
нуклеотиди;
Г пептиди.
4. Амінокислоти
відрізняються одна від одної хімічною будовою:
А аміногрупи;
Б карбоксилу;
В радикалу;
Г радикалу і карбоксилу;
Д карбоксилу і аміногрупи.
5. Рівнів
структурної організації білкової молекули існує:
А 4;
Б 3;
В 2.
6. Під
час утворення білкового полімеру відбувається зчеплення амінокислот і
виділяється речовина:
А амоніак;
Б вода;
В карбон (IV) оксид;
Г вуглеводень.
7. Третинна
структура білків має вигляд:
А глобули;
Б спіралі;
В ланцюга амінокислотних залишків.
8. Амінокислоти
у поліпептидний ланцюг сполучаються зв’язком:
А водневим;
Б пептидним;
В
ковалентним;
Г
гідрофобним.
9.
Встановіть
відповідність між білками та їх місцем знаходження:
А пепсин
1. Мʼязи;
Б гемоглобін 2.
Шлунок;
В еластин 3.
Еритроцити;
Г міоглобін
4. Шкіра.
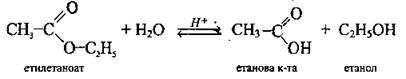



























Комментариев нет:
Отправить комментарий